Bạn đang xem: Ete là gì
Ethers (/ ˈiːθər /) là một nhóm các hợp chất hữu cơ có chứa một nhóm ether, một nguyên tử oxy được kết nối với hai nhóm alkyl hoặc aryl. Chúng có công thức chung là Rạn OTHER R, trong đó R và R ′ đại diện cho các nhóm alkyl hoặc aryl. Các ete một lần nữa có thể được phân loại thành hai giống: nếu các nhóm alkyl giống nhau ở cả hai phía của nguyên tử oxy, thì đó là ether đơn giản hoặc đối xứng, trong khi nếu chúng khác nhau, ete được gọi là ete hỗn hợp hoặc không đối xứng. Một ví dụ điển hình của nhóm thứ nhất là ete dietyl dung môi và thuốc mê, thường được gọi đơn giản là “ether” (CH3 phiên CH2 hạ O âm CH2 hạ CH3). Ethers là phổ biến trong hóa học hữu cơ và thậm chí phổ biến hơn trong hóa sinh, vì chúng là liên kết phổ biến trong carbohydrate và lignin.
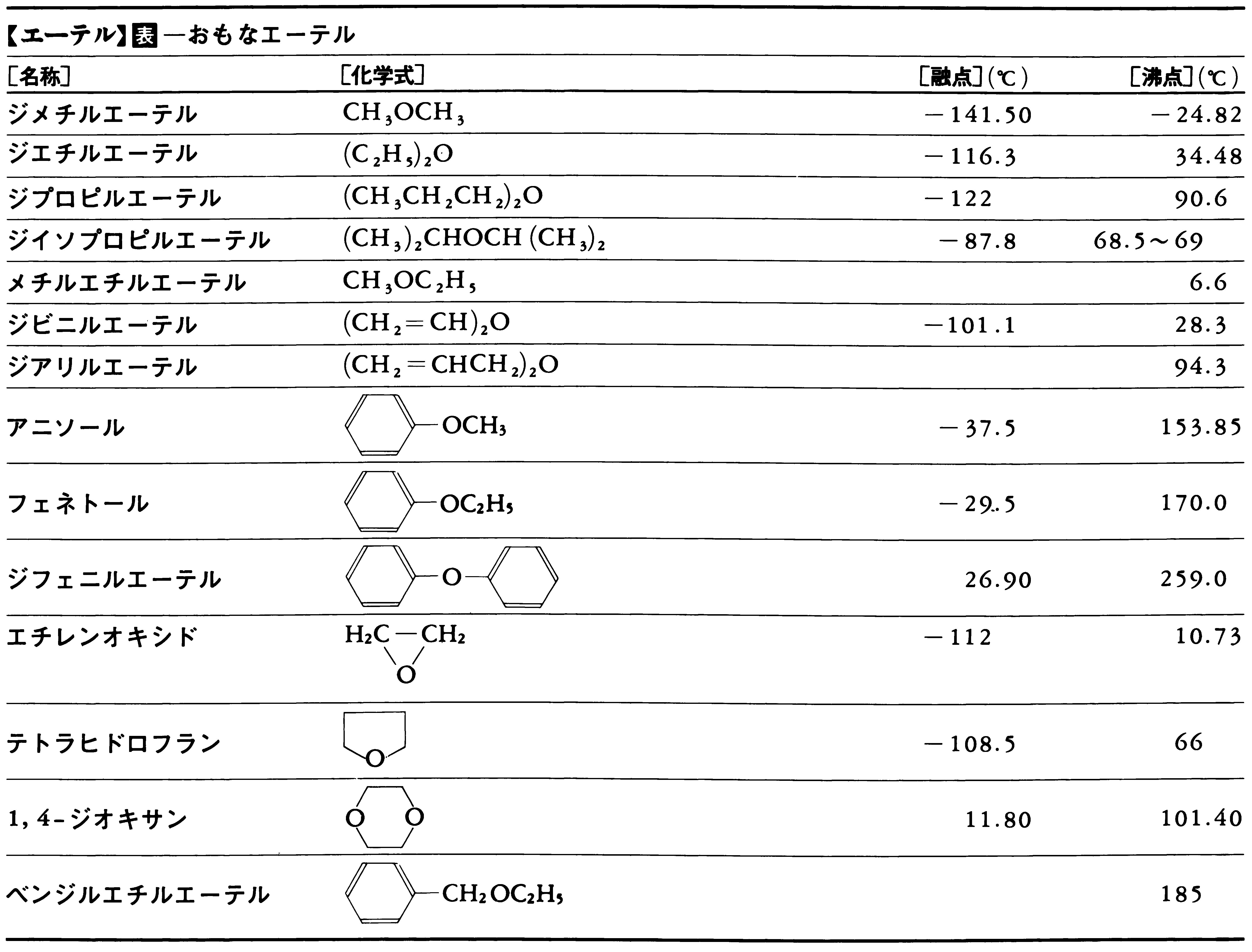
Một thuật ngữ chung cho các hợp chất hữu cơ có liên kết carbon-oxy-carbon —C CÂU CẠNH (liên kết ether). Theo nghĩa hẹp, nó cũng được sử dụng như một từ viết tắt của diethyl ether C 2 H 5 OC 2 H 5 . Thuật ngữ ether có nguồn gốc từ tiếng Hy Lạp aithēr, có nghĩa là tâm linh trên bầu trời, và được sử dụng để đặt tên cho một phương tiện gần như được coi là phương tiện để truyền ánh sáng, nhiệt, v.v.
Phân loại
Ether được biểu diễn bằng công thức chung Rơi O Sự R (R và R ′ là các nhóm alkyl hoặc nhóm aryl). R = R ‘được gọi là ether đối xứng (ether đơn) và R ≠ R’ được gọi là ether không đối xứng (ether lai). Hơn nữa, những gì có liên kết ether là một phần của vòng được gọi là ether tuần hoàn. Trong số các ete tuần hoàn, ete vòng 3 thành phần rất căng thẳng (có 3 nguyên tử trong vòng) được gọi là epoxit và có các tính chất độc nhất so với các ete khác.
Xem thêm: 079 Là Mạng Gì – # Bán Sim Số đẹp đầu Số 0798
Xem thêm: Bùn Hoạt Tính Là Gì – Bùn Vi Sinh Hoạt Tính Là Gì
Khi R và R ‘đều là nhóm alkyl, chúng còn được gọi là ete aliphatic và khi một hoặc cả hai là nhóm aryl, chúng còn được gọi là ete thơm (phenol).
Thiên nhiên
Nhìn chung, ete chủ yếu là trung tính và có mùi hương dễ chịu, nhưng một số loại cao hơn là rắn. Các ete thấp hơn thường gây ra hỏa hoạn vì chúng dễ bay hơi và có điểm chớp cháy thấp. Ít tan trong nước, ổn định hóa học, không phản ứng với natri kim loại. Mặc dù nó có khả năng kháng kiềm rất lớn nhưng nó dễ bị phân hủy bởi axit, đặc biệt là axit hydroiodic HI.
R − O R ′ + HI─ → R − OH + R′I
Ethers được sử dụng rộng rãi làm dung môi vì những thuộc tính này. Tuy nhiên, epoxit với các chủng lớn có khả năng phản ứng cao và có nhiều công dụng khác nhau làm chất trung gian để tổng hợp hữu cơ vì tính phản ứng của chúng. Mặc dù dietyl ete đã được sử dụng làm thuốc gây mê đường hô hấp từ những năm 1840, nhưng nó hiếm khi được sử dụng trong thực hành y tế gần đây vì tính dễ cháy của nó.
Chế tạo
Diethyl ether được sản xuất công nghiệp do tác dụng của axit sunfuric đậm đặc với rượu etylic C 2 H 5 OH.
2C 2 H 5 OH + H 2 SO 4 ─ → C 2 H 5 OC 2 H 5 + H 2 O + H 2 SO 4
Các ete đối xứng thấp hơn khác có thể được sản xuất tương tự từ rượu tương ứng. Các ete không đối xứng có thể được tạo ra bằng phương pháp tổng hợp ether của AW Williamson, trong đó một alkyl halide R’X (X là một nguyên tố halogen) được phép tác dụng với natri rượu RONa (hydro của nhóm hydroxyl OH của rượu được thay thế bằng natri).
Chuyên mục: Hỏi Đáp